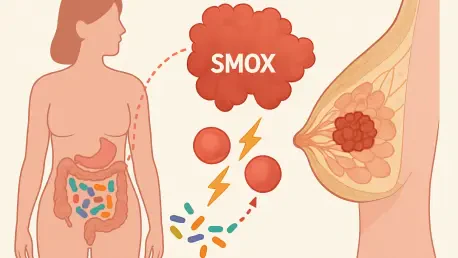
Les scientifiques explorent désormais la possibilité fascinante que l’écosystème microscopique résidant au cœur de nos intestins puisse exercer une influence déterminante sur la trajectoire clinique des tumeurs mammaires les plus agressives. Ce concept, qui semblait autrefois appartenir au domaine de la spéculation, s’appuie aujourd’hui sur des preuves moléculaires concrètes. Une étude majeure menée par des chercheurs de la Johns Hopkins University a mis en lumière un acteur biologique resté longtemps dans l’ombre : l’enzyme spermine oxydase, plus connue sous l’acronyme Smox.
Cette enzyme agirait comme un véritable transmetteur de signaux entre les déséquilibres de la flore intestinale et les cellules du tissu mammaire. En déchiffrant ce dialogue complexe, la médecine moderne commence à comprendre pourquoi certaines tumeurs progressent avec une rapidité déconcertante alors que d’autres restent plus dociles. Cette percée ne se contente pas d’élargir le champ des connaissances fondamentales ; elle redéfinit la manière dont l’oncologie perçoit l’interaction entre l’hôte et ses occupants bactériens, transformant le microbiome en un levier thérapeutique potentiel.
Une Connexion Insoupçonnée entre Nos Intestins et la Santé des Seins
L’idée qu’un déséquilibre bactérien localisé dans l’appareil digestif puisse impacter la santé d’un organe aussi distant que le sein a longtemps défié les modèles médicaux traditionnels. Pourtant, les dernières avancées démontrent que le corps humain fonctionne comme un réseau intégré où les messages chimiques circulent bien au-delà de leur zone d’émission initiale. La recherche actuelle indique que la présence de certaines bactéries pathogènes dans l’intestin ne se limite pas à provoquer des troubles gastriques, mais peut altérer profondément la biochimie des tissus périphériques.
L’enzyme Smox se trouve précisément au centre de cette communication inter-organes. En cas de dysbiose intestinale, cette enzyme est activée de manière anormale, déclenchant des processus biochimiques qui favorisent la tumorigenèse. Ce lien inattendu suggère que la santé mammaire est étroitement corrélée à l’équilibre de la microflore, une révélation qui pousse les oncologues à regarder bien au-delà de la tumeur elle-même pour comprendre les racines de la maladie.
Comprendre l’Enjeu du Microbiome dans l’Oncologie Moderne
Le cancer du sein demeure une préoccupation majeure de santé publique, et malgré l’efficacité croissante des traitements, la variabilité de la réponse thérapeutique reste un défi. L’émergence du concept de « microbiote oncogénique » apporte une réponse partielle à ce mystère. Il est désormais admis que les bactéries ne sont pas de simples spectatrices, mais des actrices capables de modifier l’environnement tumoral et d’influencer la réponse immunitaire de la patiente.
Cette influence s’exerce par le biais de métabolites et de toxines qui voyagent dans la circulation sanguine, atteignant les cellules mammaires et modifiant leur comportement. Un microbiome déséquilibré crée un terrain propice à l’inflammation chronique, un facteur bien connu pour favoriser la croissance des cellules malignes. En intégrant l’analyse du microbiome dans le cadre oncologique, la médecine s’oriente vers une approche plus globale, où chaque patiente est considérée non seulement à travers son génome, mais aussi à travers son profil bactérien unique.
La Smox : le Carrefour Moléculaire de la Tumorigenèse
L’enzyme Smox joue un rôle de pivot dans la dégradation des polyamines, mais sa suractivation devient dévastatrice pour l’intégrité cellulaire. Lorsqu’elle s’emballe sous l’influence de stimuli bactériens, elle produit des quantités massives de peroxyde d’hydrogène, plongeant les cellules mammaires dans un stress oxydatif sévère. Ce phénomène n’est pas sans conséquence : il provoque des cassures répétées dans les brins d’ADN, favorisant l’accumulation de mutations génétiques qui transforment des cellules saines en foyers cancéreux agressifs.
La bactérie Bacteroides fragilis entérotoxigène (ETBF) est particulièrement impliquée dans ce processus. En libérant ses toxines, elle stimule non seulement la Smox, mais elle provoque également une cascade inflammatoire impliquant des messagers comme l’interleukine-6 et le TNFα. Ces cytokines alimentent un cercle vicieux où l’inflammation renforce l’activité de l’enzyme, laquelle accélère en retour la prolifération tumorale. Ce carrefour moléculaire est également sollicité par d’autres agents pathogènes comme Escherichia coli ou Fusobacterium nucleatum, prouvant que divers déséquilibres microbiens peuvent mener à une même issue pathologique via la Smox.
Les Preuves Scientifiques Issues des Recherches de la Johns Hopkins University
Les travaux rigoureux publiés dans la revue Cancer Research ont apporté une validation empirique à ces mécanismes observés en laboratoire. En utilisant des modèles expérimentaux sophistiqués, les chercheurs ont pu démontrer que la colonisation par des bactéries entérotoxigènes entraînait systématiquement une augmentation de la taille des tumeurs et une fréquence accrue des métastases. Les données montrent une corrélation directe entre la charge bactérienne pathogène et la sévérité clinique de la maladie mammaire.
L’aspect le plus probant de cette recherche réside dans l’expérimentation de blocage enzymatique. En utilisant des molécules capables d’inhiber spécifiquement la Smox, les scientifiques ont réussi à neutraliser l’effet pro-tumoral induit par les bactéries. Cette réussite confirme que l’enzyme est bien le maillon essentiel de la chaîne. Ces résultats offrent une preuve de concept solide : manipuler cette voie métabolique permet de modifier l’évolution naturelle du cancer, ouvrant ainsi des perspectives inédites pour le développement de nouveaux protocoles de soins.
Stratégies d’Application et Perspectives pour les Patientes
L’identification de la Smox comme médiateur clé entre le microbiote et le cancer du sein permet d’envisager des stratégies de dépistage beaucoup plus fines. À l’avenir, l’analyse du profil microbiotique intestinal pourrait être intégrée aux bilans de routine pour évaluer le risque de progression rapide chez les patientes diagnostiquées. Détecter précocement la présence de souches comme l’ETBF permettrait une intervention ciblée bien avant que les dommages génomiques ne deviennent irréversibles.
Sur le plan thérapeutique, l’introduction d’inhibiteurs de la Smox dans l’arsenal oncologique représente un espoir concret. Utilisés en complément des traitements conventionnels comme la chimiothérapie, ces médicaments pourraient protéger les cellules saines du stress oxydatif tout en freinant la croissance des cellules malignes alimentées par la dysbiose. Cette approche pluridisciplinaire, combinant oncologie et microbiologie, a ouvert la voie à une personnalisation accrue des soins, où l’on ne traite plus seulement la tumeur, mais l’ensemble de l’écosystème biologique de la patiente pour garantir de meilleurs résultats cliniques.
Les découvertes ont ainsi établi un lien irréfutable entre la flore intestinale et la virulence des tumeurs mammaires, marquant un tournant dans la recherche médicale. Les équipes de la Johns Hopkins University ont apporté des preuves montrant que l’enzyme Smox constituait le carrefour où l’inflammation bactérienne rencontrait l’instabilité génétique. Ces travaux ont suggéré que la manipulation du microbiome et l’inhibition enzymatique deviendraient des piliers de la prévention. Les cliniciens ont alors commencé à envisager des protocoles où la santé digestive et l’oncologie mammaire étaient traitées de concert. Cette perspective a transformé l’approche thérapeutique, plaçant la surveillance bactérienne au cœur de la lutte contre la progression du cancer du sein.